Profesor Wojciech Święszkowski opowiada o zwycięskim bioimplancie
W kwietniu 2015 r. zespół prof. Wojciecha Święszkowskiego został uhonorowany nagrodą Luminatus 2015. O charakterze nagrodzonego projektu i jego wdrażaniu profesor opowiada w rozmowie z Biuletynem Politechniki Warszawskiej.
Jak czytamy na stronie macierzystej projektu: Bio-Implant ma charakter interdyscyplinarny. Współpracują przy nim zespoły posiadające odpowiednie doświadczenie oraz bazę badawczą w zakresie medycyny, biologii, inżynierii materiałowej, technik wytwarzania CAD/CAM oraz informatyki.
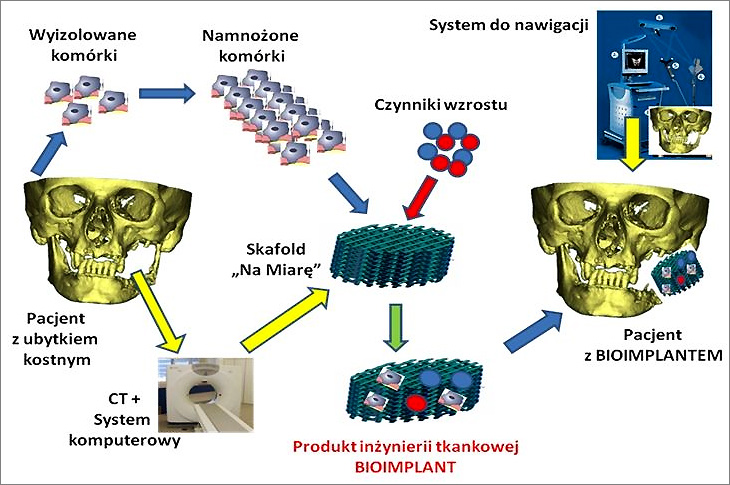
Celem projektu jest opracowanie i przygotowanie do wdrożenia nowatorskich produktów inżynierii tkankowej (bioimplantów) wspomagających regenerację i odtworzenie rozległych ubytków tkanek kostnych, które powstają w wyniku usuwania nowotworu. W efekcie ma powstać gotowa do wdrożenia w praktyce, kliniczna metoda leczenia onkologicznych ubytków kostnych w okolicy twarzoczaszki człowieka z zastosowaniem innowacyjnego produktu inżynierii tkankowej oraz komputerowych systemów wspomagania operacji.
Zespół projektowy tworzą eksperci i praktycy z Politechniki Warszawskiej, Centrum Onkologii - Instytutu im. Marii Curie-Skłodowskiej, Politechniki Wrocławskiej oraz Warszawskiego Uniwersytetu Medycznego. Jego kierownikiem jest prof. Wojciech Święszkowski z Wydziału Inżynierii Materiałowej PW, który przyznaje, że już na studiach doktoranckich wraz z grupą kolegów i lekarzami opracował swoją pierwszą endoprotezę. Wówczas była to endoproteza głowy kości promieniowej (fragment stawu łokciowego), opatentowana i wdrożona do produkcji.
Impuls w kierunku badań nad bioimplantem wyszedł natomiast od doktora Jaworowskiego, chirurga rekonstrukcyjnego, który pięć lat temu pojawił się w gabinecie prof. Święszkowskiego. Co się zmieniło od tamtej pory? Odpowiedzi na to pytanie dostarcza rozmowa z prof. Wojciechem Święszkowskim.
Na jakim etapie realizacji jest projekt?
Oficjalnie projekt zakończył się we wrześniu 2014 r. Można powiedzieć, że niestety, bo zakończyliśmy go na etapie wstępnych badań na zwierzętach. Nasze bioimplanty były wszczepiane w żywe struktury, a konkretnie w model owcy, gdzie był wygenerowany ubytek krytyczny w żuchwie. Właśnie tam wszczepialiśmy nasz bioimplant zasilany komórkami macierzystymi pochodzącymi z owcy. Wyglądało to tak, że tkanka kostna formowała się w ubytku wygenerowanym wewnątrz skafoldu. Z biegiem czasu rusztowanie powoli się rozpuszczało. W efekcie ma pozostać jedynie uformowana tkanka kostna, bez dodatkowego materiału syntetycznego w postaci kompozytu. Można powiedzieć, że eksperyment zakończył się sukcesem już po 3 miesiącach, bo taki był zaplanowany okres wstępnej obserwacji.
Słyszałam, że komórki macierzyste najczęściej pobierane są z komórek tłuszczowych?
Taki jest teraz trend, choć są różne źródła ich pochodzenia. Trzeba pamiętać, że komórki macierzyste mają zdolność do tworzenia różnych tkanek tylko wtedy, jeśli są odpowiednio pobudzone do tego działania. Tradycyjną, choć nieco uciążliwą, lecz nadal stosowaną metodą, jest pobieranie ich ze szpiku kostnego. Jednocześnie tych komórek jest niestety mniej, a przy dużych ubytkach potrzebujemy ich całkiem pokaźną ilość. W ostatnich latach okazało się, że tkanka tłuszczowa jest bardzo dobrym zasobnikiem komórek macierzystych również do odtwarzania kości. Ponadto liposukcja jest metodą znaną od wielu lat i po pewnych modyfikacjach może być używana do pobierania materiału służącego do izolacji komórek macierzystych.
A jeśli chodzi o odżywianie implantu. Czy pacjentom będą podawane specjalne preparaty pozwalające na lepsze namnażanie się tkanek?
Proces regeneracji wymaga pewnych bodźców. Wśród nich możemy wymienić czynniki wzrostu. Oczywiście występują one w naszym organizmie i będą pobudzane do działania przez komórki macierzyste, lecz w niektórych przypadkach przewidujemy, że takie czynniki wzrostu będą dostarczane w miejsce leczenia.
Wewnętrzny szkielet ulega biodegradacji. Czy istnieje zatem jakiekolwiek prawdopodobieństwo, że jego rozpuszczone pozostałości wywołają alergię?
Takie zagrożenie przewidziano dla każdego materiału medycznego, nawet jeśli jest uznany przez wszystkie organizacje jako materiał całkowicie biozgodny. Odpowiedniki materiałów używanych przez nas w bioimplantach można znaleźć np. w resorbowalnych szwach chirurgicznych, które są przyswajalne przez nasz organizm. Na modelach zwierzęcych również nie mieliśmy problemów z odrzuceniem tego materiału.
Dlaczego przy uzupełnianiu ubytków bioimplantem skupiliście się Państwo jedynie na okolicach twarzoczaszki?
Projekt został skierowany w okolice twarzoczaszki z dwóch względów. Po pierwsze, jest to nowotwór i nie ma innej metody leczenia, jak jego usunięcie. Powstaje wtedy duży ubytek, który w tej okolicy jest szczególnie widoczny. Cierpieniu związanemu z chorobą onkologiczną towarzyszy w tym wypadku także upośledzenie wizerunku pacjenta, stąd nasz pomysł, by skoncentrować się właśnie na tym obszarze. Stanowi to duże wyzwanie, bo pomimo tego, że są to okolice twarzoczaszki, bardzo trudna jest regeneracja żuchwy. Mniejszym wyzwaniem jest leczenie oczodołów, które występują w tej okolicy, czy regeneracja ubytków w pokrywie czaszki. Są to bowiem fragmenty mniej obciążone mechanicznie. Nasze doświadczenie pozwala równocześnie sugerować regenerację tkanki kostnej w innych miejscach układu szkieletowo-mięśniowego np. w okolicy kości długich, czy kości krótkich. Są to podobne zagadnienia. I choć struktura kości jest inna, mikrostruktura podłoża dla tych komórek jest podobna. To tylko kwestia modyfikacji geometrii, ale i ona nie jest problemem, kiedy używamy techniki druku 3d.
Na czym zatem polega wspomaganie komputerowe?
Wspomaganie komputerowe stanowi obecnie nieodzowny element projektowania nowych produktów medycznych, począwszy od projektowania samej geometrii implantu. By właściwie wypełnić ubytek, bioimplant jest robiony „na miarę”. Jednocześnie jesteśmy w stanie projektować właściwości używanych biomateriałów, aby zapewnić odpowiednią wytrzymałość konstrukcji implantu. Korzystając z nowoczesnych metod modelowania matematycznego i symulacji komputerowej jesteśmy też w stanie przybliżyć, co będzie się później działo z tym bioimplantem w żywym organizmie.
Projekt zakończyła faza testów na zwierzętach. Kiedy możemy spodziewać się wdrożenia tej metody u ludzi?
Projekt od samego początku był skierowany na leczenie ubytków tkanki kostnej u chorych onkologicznie. Droga jaką musi on przebyć jest typowa dla każdego nowego produktu medycznego czy też nowej metody. Po żmudnej pracy w laboratorium następują badania in vitro, gdzie na samych liniach komórkowych należy wykazać brak cytotoksyczności i pewną wstępną biozgodność, gdyż prawdziwą biozgodność możemy ocenić dopiero na modelu zwierzęcym. Dopiero później przechodzi się do badań na zwierzętach. Kolejnym krokiem, który mamy zaplanowany w ramach ubiegania się o środki finansowe są badania kliniczne I fazy, czyli badania bezpieczeństwa naszego rozwiązania na wybranych ochotnikach tj. pacjentach.
A czy na zwierzętach można już oficjalnie stosować bioimplanty?
Naprawialiśmy ostatnio nogę Zuzi, dużego psa z łapą objętą nowotworem. W jej przedniej części duży fragment tkanki kostnej został usunięty przez weterynarza. My wszczepiliśmy tam bioimplant. Jednak aby ta metoda była szerzej powszechna, potrzebny jest jeszcze cały szereg badań. W tym konkretnym przypadku i po pozytywnych wynikach eksperymentu na owcach, właściciele psa wyrazili zgodę na taki zabieg. Poza nim jedyną dostępną alternatywą była amputacja kończyny. Jak na razie nasza metoda się sprawdza, a kość wrasta już trzy miesiące. W przyszłym roku prawdopodobnie wszystkie procedury medyczne dla zwierząt mają być dopuszczane na takich samych zasadach, jak te dla ludzi. Nasz bioimplant także będzie musiał przejść dodatkowe próby kliniczne.
Czy gdzieś na świecie prowadzone są podobne badania?
Owszem. Jestem z tymi ludźmi w bieżącym kontakcie. Wymieniamy się spostrzeżeniami, wynikami, spotykamy się na konferencjach. Na szczęście, projekt jest prowadzony równolegle w wielu krajach. Regeneracja tkanki kostnej stanowi bowiem bardzo ważny problem, na którym koncentruje się kilka grup. Jesteśmy naukowcami, cieszymy się, że z naszych wyników może ktoś skorzystać. Ważne jest, aby postęp szedł do przodu i żeby te metody wkroczyły na pole medyczne w szerokim zakresie. Tym samym będą one dostępne dla każdego pacjenta, a nie tylko dla wybranych.
Nagroda widzę stoi w pokoju?
Tak, obiecałem zespołowi, że przez pół roku pozostanie w Politechnice Warszawskiej. Za sześć miesięcy przejdzie do innej instytucji.
Dziękuję za rozmowę!
Rozmawiała: Izabela Koptoń-Ryniec
Podobny artykuł:
Zespół pracujący nad projektem Bio-Implant nagrodzony Luminatus 2015
W telewizji:
Panorama z dnia 19 maja 2015 godz.18.00 (25:52 do 26:07)
Zdjęcia: IKR/Biuletyn PW, materiały Projektu Bio-implant